Рубрика: Новини
Международен екип от учени, включващ изследователи от Медицински университет – София, установи нов биологичен механизъм, който обяснява различията в развитието на мозъка при индивиди със синдром на Даун. Съвместното проучване, в което участват още Медицинският факултет „Икан“ (Mount Sinai), Институтът за изследване на мозъка „Либер“ и Университетът на Аризона, е публикувано в престижното научно списание Nature Communications.
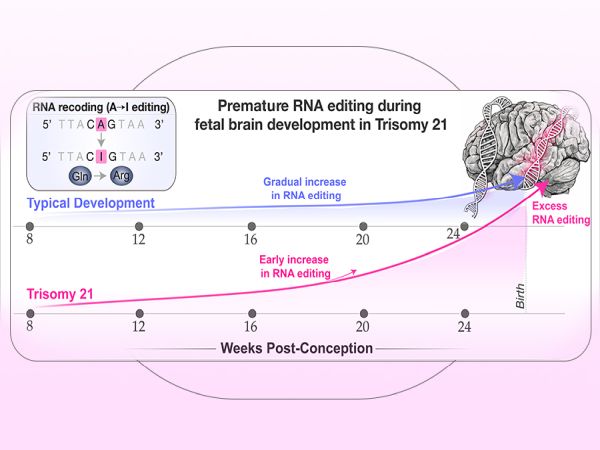
Резултатите от изследването сочат, че свръхпроизводството на ензима за РНК редакция ADARB1 (познат и като ADAR2) води до преждевременни и прекомерни изменения в РНК транскриптите на развиващите се мозъчни клетки. Тази аномалия засяга пряко начина, по който невроните комуникират помежду си и изграждат невронни мрежи. Синдромът на Даун, или тризомия 21, се характеризира с наличието на допълнително копие на хромозома 21. Досега беше известно, че тази генетична особеност влияе върху развитието, но точните механизми на ранното мозъчно формиране оставаха неизяснени.
Според доц. Майкъл С. Брийн от Mount Sinai, допълнителната хромозома причинява генетичен дисбаланс, който повишава нивата на този ключов ензим. Процесът на РНК редакция е естествен и жизненоважен за финото настройване на протеиновите функции в невроните по време на ранното развитие. При тризомия 21 обаче той протича твърде рано и в много по-широк мащаб, което компрометира правилното формиране на синаптичните връзки от самото начало.
Изследователският екип е анализирал фетална мозъчна тъкан от критичния период между 13-ата и 22-рата гестационна седмица. Проектът е реализиран чрез тъканни проби от Центъра по молекулна медицина (ЦММ) към МУ-София и Института „Либер“, обхващайки 20 индивида с тризомия 21 и 27 в контролната група. Фокусът е поставен върху префронталния кортекс и хипокампуса – зони, отговарящи за паметта и когнитивните функции. Чрез РНК секвениране от ново поколение е установено мащабно нарушение в генната експресия, като генът ADARB1 от хромозома 21 показва най-често повишена активност.
Особено важно откритие е свръхредакцията в ключови гени като GRIA2, GRIA3, GRIK2 и GABRA3. Те кодират глутаматните и GABA рецепторите, които регулират предаването на сигнали между невроните. Това води до прекодиране на РНК и промяна в аминокиселинната последователност на синтезираните протеини, което директно модифицира тяхната функция. Учените предполагат, че тези ранни молекулярни изменения нарушават баланса между възбуждащата и инхибиторната сигнализация в критичния момент на изграждане на невронните мрежи. Данните са безспорно потвърдени чрез допълнителен анализ на девет независими бази данни за човешка тризомия 21.
Откритието предефинира невропатологията на синдрома на Даун, посочвайки РНК редакцията като измерим биомаркер за ранното развитие на нервната система и обещаваща мишена за терапевтични интервенции. Както отбелязва проф. Радка Кънева, ръководител на ЦММ към МУ-София и ководещ изследовател от българска страна: „Това проучване разкрива фундаментални молекулярни механизми и поставя нови основи за бъдещи изследвания и иновативни подходи в разбирането и подкрепата на пациентите със синдром на Даун.“