 През последните години наблюдаваме динамично развитие на един иновативен подход в лечението на онкологични заболявания, а именно противотуморната имунотерапия. В основата си този тип лечение има за цел да стимулира собствената имунна система на пациента, която ефективно да атакува раковите клетки. И макар тази концепция да води началото си от края на 19-ти век, с наблюденията на Уилиям Коули, едва наскоро беше припознато потенциалното ѝ значение за медицината и през 2013 година списание Science обяви противотуморната имунотерапия за откритие на годината.
През последните години наблюдаваме динамично развитие на един иновативен подход в лечението на онкологични заболявания, а именно противотуморната имунотерапия. В основата си този тип лечение има за цел да стимулира собствената имунна система на пациента, която ефективно да атакува раковите клетки. И макар тази концепция да води началото си от края на 19-ти век, с наблюденията на Уилиям Коули, едва наскоро беше припознато потенциалното ѝ значение за медицината и през 2013 година списание Science обяви противотуморната имунотерапия за откритие на годината.
Основните етапи в имунния отговор на организма спрямо туморните клетки се обобщават в така наречения противотуморен имунологичен цикъл.
Първият сигнал, който задейства този цикъл, се обуславя от самото естество на онкогенезата и формирането на неоантигени, специфични за тумора: мутирали или свръх-експресирани протеини, които се отделят от раковите клетки.
Имунната система разпознава тези антигени и използва антиген презентиращи клетки (АПК), за да ги предостави за разпознаване и активира Т-лимфоцитите в лимфните възли. Процесът на активация или „прайминг“ на Т-лимфоцитите се обуславя от няколко фактора: 1) свързване с антигена посредством Т-клетъчен рецептор (TCR); 2) ко-стимулиращ сигнал (B7:CD28); 3) цитокини. Активацията на Т-лимфоцитите се регулира внимателно от имунната система и позволява фина настройка на имунния отговор: свръхактивацията би довела до автоимунна реакция, и обратното – недостатъчната активация би ускорила развитието на рака.
Веднъж активирани, Т-лимфоцитите напускат лимфните възли, попадат в кръвния ток, мигрират през ендотела и достигат до тумора. Там те трябва да разпознаят специфичния антиген на повърхността на туморната клетка, който е свързан с главен комплекс на тъканна съвместимост I (MHC I). Това взаимодействие е от изключителна важност, за да могат Т-лимфоцитите да проявят своята цитотоксична дейност, но и тук редица фактори могат да стимулират или инхибират активността им.
В последния етап от противотуморния имунологичен цикъл Т-лимфоцитите изпълняват програма за клетъчна цитотоксичност като освобождават цитотоксини – перфорин, гранзими и гранулизин, които задействат апоптоза на раковата клетка, отделяйки големи количества неоантигени в средата, затваряйки цикъла.
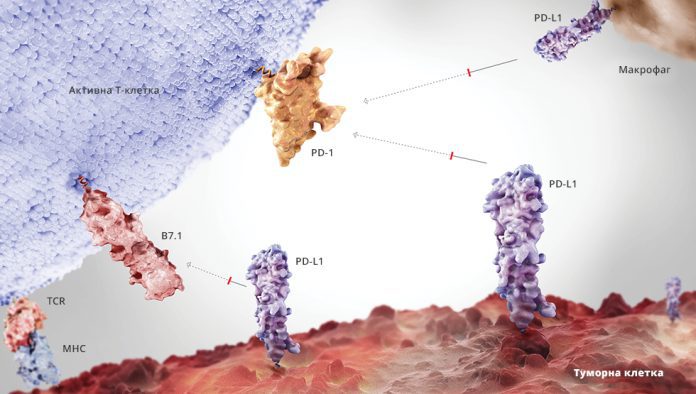
В процеса на онкогенеза раковите клетки негативно повлияват някоя (или няколко) от посочените стъпки (т.нар. чекпоинти, checkpoints) и така саботират имунната система, като не позволяват пълноценен имунен отговор. Един такъв механизъм, който раковите клетки успешно използват, е взаимодействието между протеина за програмирана смърт 1 (PD-1) и неговия лиганд (PD-L1). PD-1 е мембранен протеин, който се експресира от клетки на имунната система – активирани Т-лимфоцити, моноцити и дендритни клетки. PD-L1 от своя страна също се експресира от клетки на имунната система, но и от туморни клетки. Взаимодействието между PD-L1 и PD-1 има регулаторна функция и при нормални условия води до инхибиране на активността на T-лимфоцитите и предпазва организма от свръхактивност на имунната система и нежелани автоимунни реакции.
Експресията на PD-L1 от туморните клетки инхибира активността на цитотоксичните Т-лимфоцити в туморната среда и блокира ефективния имунен отговор. В опит да бъде възстановена ефективността на имунния отговор, през последните години бяха разработени и одобрени няколко агента – чекпoинт инхибитори (checkpoint inhibitors), които блокират взаимодействието PD-1/PD-L1, водейки до ефективното възстановяване на антитуморния имунен отговор.
Освен с PD-1, PD-L1 взаимодейства още и с друг мембранен протеин – B7-1 (също CD20), който се експресира най-вече от дендритни клетки, и взаимодействието между двата протеина има инхибиторен ефект върху активацията на Т-лимфоцитите в лимфните възли. Блокирането на PD-L1, но не и на PD1, прави невъзможно взаимодействието PD-L1 – B7-1 и свободният B7-1 може да се свърже с друг рецептор по повърхността на Т-лимфоцитите – CD28, взаимодействие, което стимулира тяхната активация.
Туморната ангиогенеза е друг важен фактор от ключово значение за връзката между тумора и имунния отговор. Съдово-ендотелният растежен фактор (VEGF) има важнa роля в неоваскуларизацията на тумора и има редица имуносупресивни ефекти: потиска съзряването на дендритните клетки, както и стимулира експресията на PD-L1. От друга страна, инфилтрацията и екстравазацията на Т-лимфоцитите пряко зависят от адхезията им към ендотела на кръвоносните съдове, но експресията на VEGF и други фактори инхибират експресията на адхезионни молекули в клетъчния ендотел.
Поради важното значение на VEGF/VEGFR, бяха разработени редица инхибитори, които успешно се използват в лечението на различни видове рак. Комбинацията от VEGF и – чекпоинт инхибитори като комбинирана терапия представлява особен интерес, тъй като блокирането на VEGF има потенциала да подобри инфилтрацията на Т-лимфоцитите в туморната среда и по-висока ефективност на имунотерапията.
Свидетели сме на истинска революция в лечението на раковите заболявания. През следващите години очакваме резултати от важни клинични изпитвания, които биха довели до налагането на съвсем нов подход в лечението на онкологичните заболявания.
Референции:
Richardson MA, Ramirez T, Russell NC, et al. Altern Ther Health Med 1999;5:42-7; Science, vol 342, 20 December 2013; Chen DS, Mellman I., Immunity 2013;39:1–10; Keir ME, et al. Annu Rev Immunol 2008; Park JJ, et al. Blood 2010; Chen DS, et al. Clin Cancer Res 2012; Rozali, et al. Clin Dev Immunol 2012; Topalian SL, et al. New Engl J Med 2012; Latchman Y. et al. Nat Immunol 2001; Matsumoto K, et al. Biochem Biophys Res Commun 2008; Brahmer JR, et al. J Clin Oncol 2010; Akbari O, et al. Mucosal Immunol 2010; Collins M, et al. Genome Biol 2005; Murphy K, et al. Janeway’s Immunobiology 2012; Ott et al. Front Oncol. 2015; 5: 202.